نانو و آند باتری 3-آند LTO
در این مقاله آندهای خانواده اکسید تیتانیوم معرفی و اثرات نانو بر ارتقای عملکرد این آندها بیان میشود و در آخر رفتار شبه خازنی که خاص نانوست، معرفی خواهد شد. اگرچه در این مقاله اثرات مثبت نانو در ارتقای عملکرد باتری گفته میشود، درباره ماهیت شیمی-فیزیکی اتفاقات رخ داده در ابعاد نانو بحث نمیشود و به مطالب تکمیلی ارجاع داده میشود.
این مقاله شامل سرفصلهای زیر است:
1- معرفی آند LTO
2- آند TiO2
3- ظرفیت شبه خازنی
4- جمعبندی و نتیجهگیری
1- معرفی آند LTO
تا بهحال درباره دو نوع آند گرافیت و آندهای آلیاژی (سیلیکون) در مقالات قبلی صحبت شد. آند دیگری که خیلی مورد توجه است آندی با ترکیب Li4Ti5O12 است که به اختصار LTO نامیده میشود. این آند همانند گرافیت از نوع درجی (Intercalation) است. شکل 1 ساختار و واکنش این نوع آند را نشان میدهد.
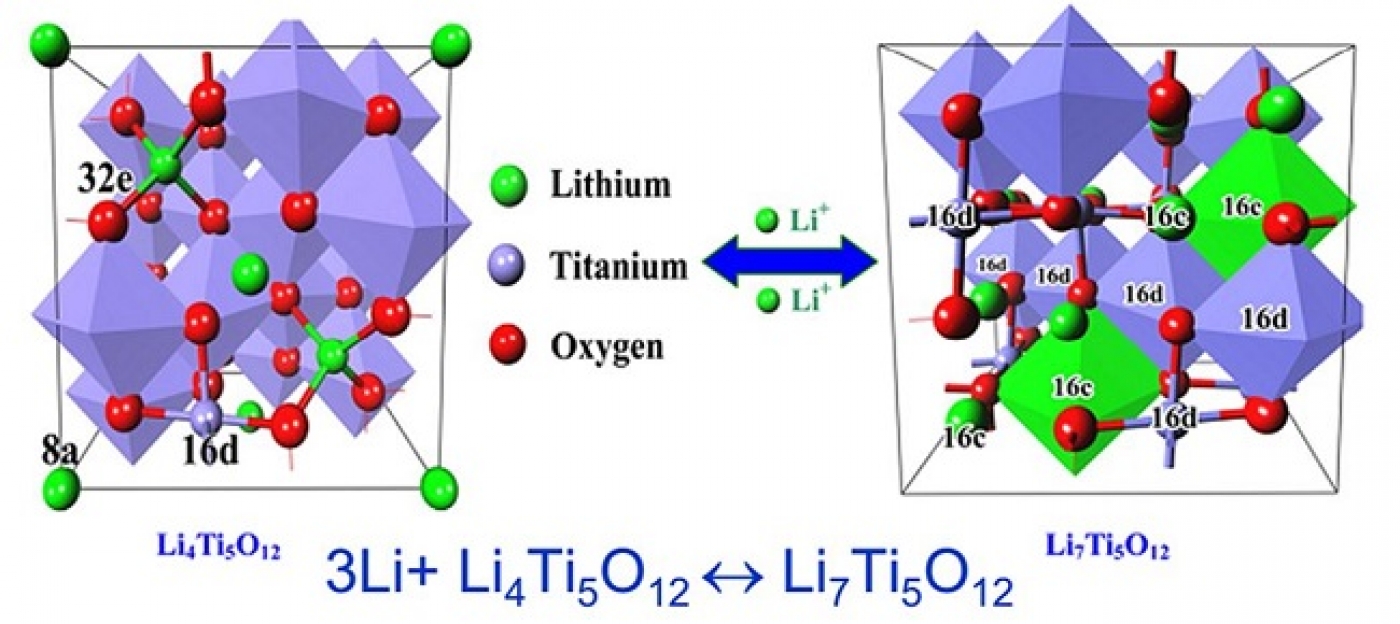
شکل 1- نمایش ساختار و نحوه ورود یون لیتیوم در LTO همراه با واکنش آن.
آند LTO دارای ظرفیت محدود 175mAh/g است (در مقایسه با 300 گرافیت و 4000 سیلیکون). ولتاژ این آند نیزمطابق شکل 2 در حدود 1.5 ولت نسبت به فلز لیتیوم است (هر چه ولتاژ آند کمتر باشد، ولتاژ باتری بیشتر میشود). این ولتاژ بالا و ظرفیت کم هر دو موجب میشوند این آند انرژی خیلی پایینی داشته باشد ولی با این همه از جنبه تجاری یک قدم جلوتر از سیلیکون است. مهمترین ویژگیهایی که موجب شده این آند مورد توجه باشد یکی بحث ایمنی است، چون در خودروهای الکتریکی شرایط غیرقابل پیش بینی وجود دارد، و دیگر طول عمر سیکلی بالا، و در آخر توان آن.
با توجه به اینکه ولتاژ این آند بالاست، مطابق شکل 2 در محدوده پایداری الکترولیت قرار میگیرد بنابراین SEI تشکیل نمیشود. از طرفی همانگونه که در شکل 1 نشان داده شده در این ترکیب فضای کافی برای قرارگیری یون لیتیوم وجود دارد و تغییر حجم نمیدهد، در حالیکه حتی در گرافیت نیز مقداری تغییر حجم در اثر ورود و خروج لیتیوم دیده میشود. بر خلاف دو آند قبلی، در این آند یون لیتیوم (نه اتم لیتیوم) ذخیره میشود و واکنش اکسیدایش ناشی از تبدیل تیتانیوم 3 به 4 ظرفیتی است نه مربوط به تغییر ظرفیت لیتیوم.
این باتری چون نه SEI دارد و نه تغییر حجم میدهد ظرفیت را به خوبی حفظ و طول عمر سیکلی بسیار بالایی (بیشتر از گرافیت) درحدود 20000 سیکل دارد. چون یک ترکیب اکسیدی است و بدلیل عدم تغییر حجم، بسیار ایمن است. چون SEI ندارد توانش هم بد نیست، فقط ضریب نفوذ یون لیتیوم پایین و رسانش الکترونی آن ضعیف است. برای حل این موضوع نانوساختارهای LTO را تهیه میکنند. چون این آند از اول SEI نداشت، وقتی نانو شود مشکل تشکیل SEI بیشتر، در نتیجه فعالیت بیشتر نانومواد را ندارد.
مشاهده شده که نانو شدن باعث میشود آند LTO ظرف 5 دقیقه (12C) شارژ و دشارژ شود. برای تهیه نانوساختار ابتدا نانوساختار اکسید تیتانیوم را تهیه کرده و سپس در معرض حرارت با یک ماده منبع لیتیوم واکنش میدهند. این موضوع نیز یک حسن LTO است، چون تهیه نانوساختارهای TiO2 بسیار معروف و شناخته شده است. با توجه به مشکل چگالی حجمی کم و آگلومره شدن نانومواد، ذرات ثانویه میکرونی ساخته شده از ذرات اولیه نانوسایز مفیدتر است (برای اطلاعات بیشتر رجوع شود به مقاله نانو و آند 2). در شکل 2 قسمت a این نانوساختار نشان داده شده است. همانطور که دیده میشود از اجتماع کنترل شده ذرات کوچکتر با ابعاد 10 نانومتر، ذرات بزرگتر میکرونی شکل گرفته است. با توجه به مقایسه قسمت b و c در شکل 2 کاملا مشخص است که این نانوساختار بر ذرات میکرونی معمولی برتری دارد، چون هم ظرفیت و هم اورپتانسیل (خصوصا در دشارژ) کمتری دارد. از این آند نانوساختار، یک باتری ساخته شده است و مشاهده شده که این باتری در مقایسه با باتری با آند گرافیتی هم از جهت طول عمر سیکلی و هم از جهت توان برتری دارد که به خاطر اختصار این منحنیها آورده نشده است. از این مطالب درباره محاسن نانو LTO در مقالات فراوان و ثابت شده است ولی آنچه باعث برتری میشود یک بحث مهم مهندسی مناسب ساختار، روش سنتز مناسب و چگونگی استفاده از ماده رسانا برای بهبود رسانایی است تا بهبود بیشتری حاصل شود، که درباره آن در مقالات آتی صحبت خواهد شد. بهعلاوه در اینکه نانو شدن برای LTO مفید است بحث نیست، ولی خیلی از پدیدههایی که در مقیاس نانو برای LTO اتفاق میافتند مورد بحث و بررسی هستند به طوری که بعضی کاملا شناخته تشدهاند (یک مثال بند پایین).
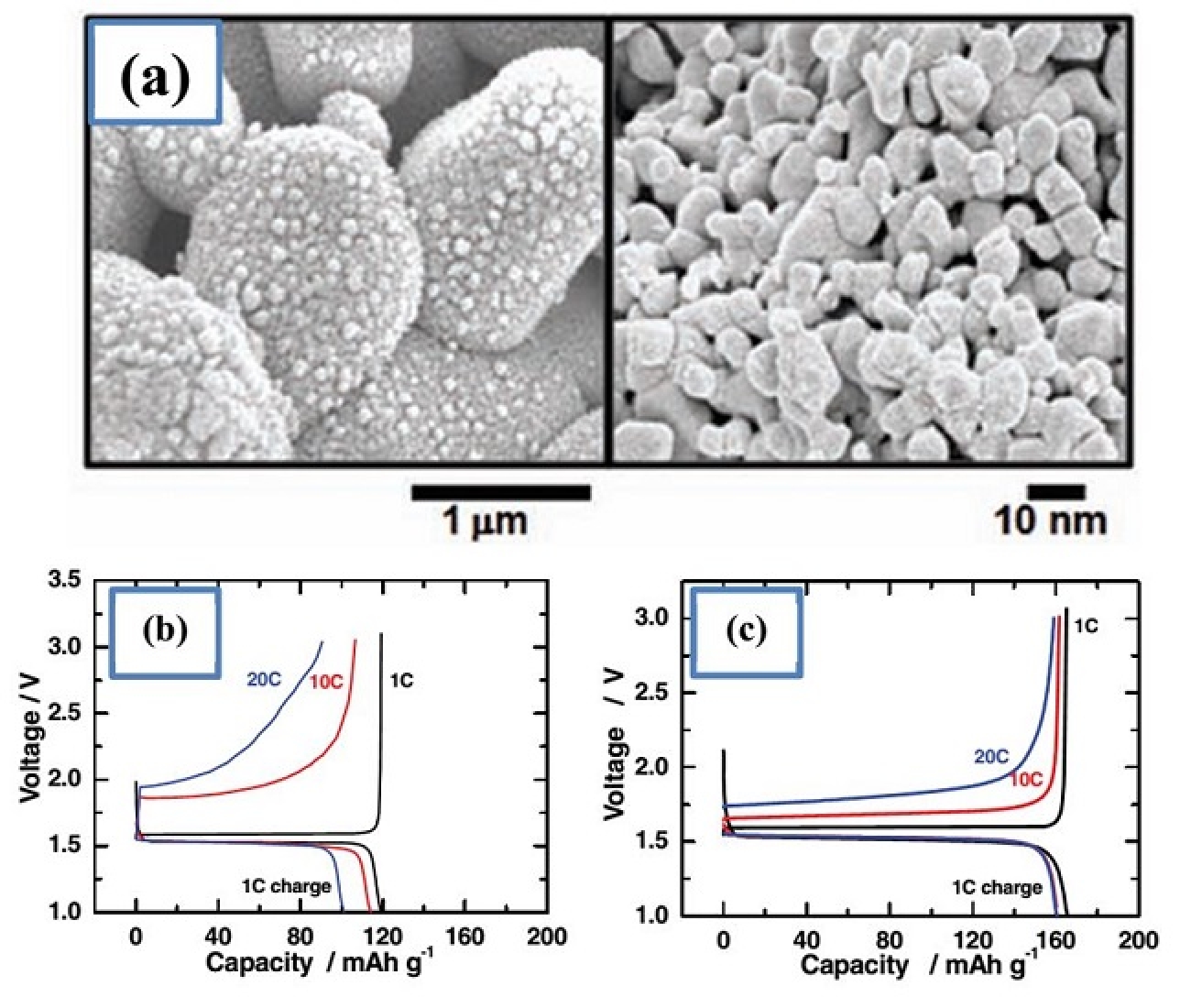
شکل 2-a- نمایش نانوساختار مورد بحث شامل نانوذرات اولیه نانو، b- منحنی شارژ-دشارژ برای میکروذرات معمول، و c- برای ذرات شکل a
یکی از اتفاقات دیگری که در ابعاد نانو رخ میدهد تغییر منحنیهای شارژ-دشارژ در برای آند LTO است. همانطور که در مقاله دوم باتری در بخش منحنیهای شارژ- دشارژ گفته شد و در شکل 3 نیز مشاهده میشود، این آند در محدوده وسیعی از ظرفیت، ولتاژ ثابتی را (کادر قرمز رنگ شکل 3) ارایه میدهد. وقتی ایعاد LTO نانو میشود ناحیه ولتاژ ثابت کاهش مییابد تا اینکه بعد از یک حد بحرانی (در رنج چند نانومتر) ناحیه ولتاژ ثابت دیگر وجود ندارد. بدلیل محدودیت حجم مطالب این مقاله، نمیتوان علتهایی که برای این پدیده گفته شده را ذکر کرد. بحث مفصلتر در مقاله کاتد LiFePO4 که این پدیده در آن هم وجود دارد، بیان میشود.
یکی از اتفاقاتی که در سطح میافتد درج بیشتر یون لیتیوم در لایههای سطحی است. در سطح بعد از درج به فرمول Li8.5Ti5O12 میرسیم که 1.5 مول بیشتر از لایههای درونی با فرمول Li7Ti5O1 است، ولی در ماده میکرونی چون درصد سطح زیاد نیست، خیلی اثر خود را نشان میدهد ولی برای نانو چون مقدار سطح به حجم فراوان است تاثیرات متعددی بر منحنی شارژ-دشارژ دارد (ارتباطات به بحث بند بالا دارد).
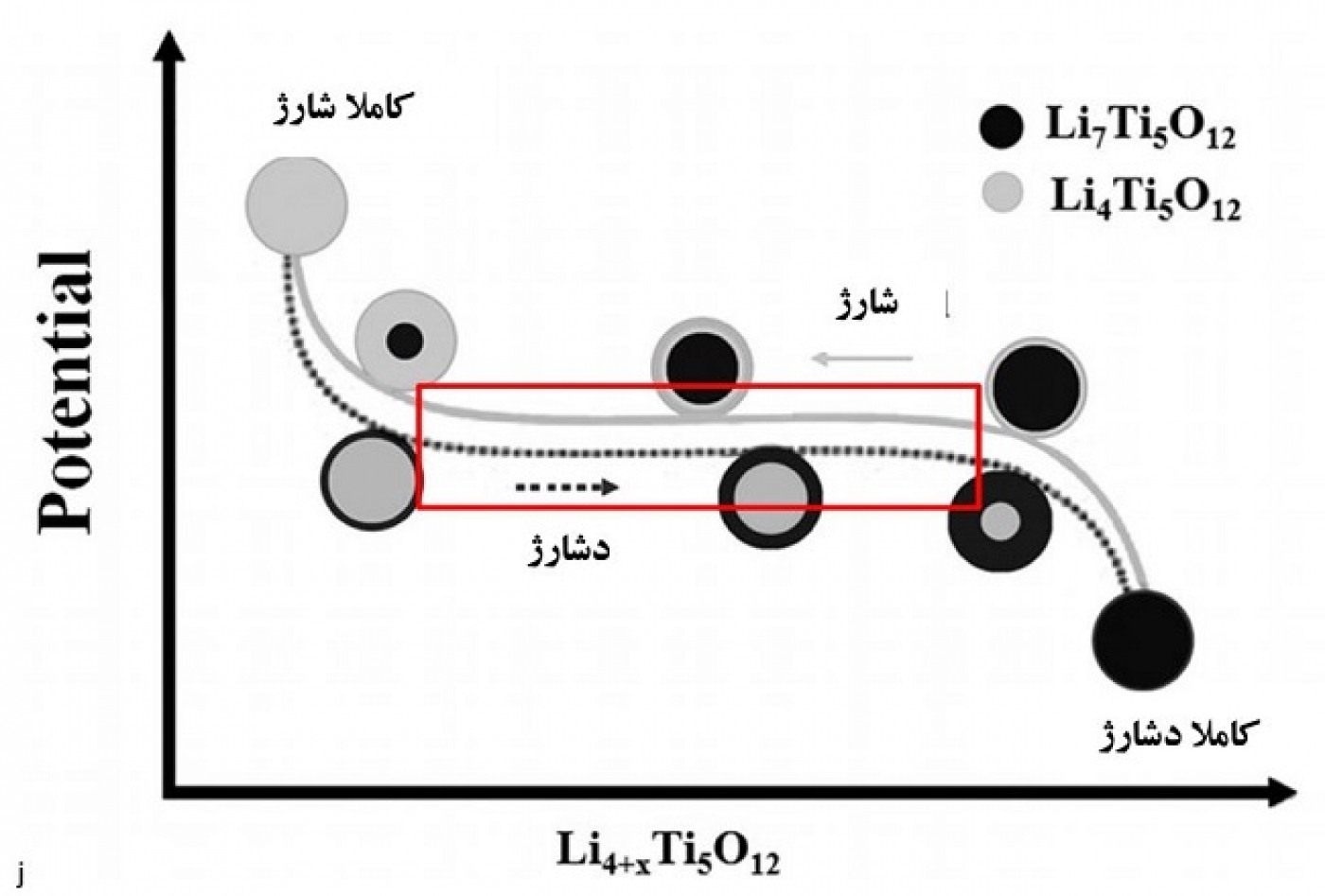
شکل 3- نمایش محدوده منحنی خطی در آند LTO در محنی شارژ-دشارژ
2- آند TiO2
از همان خانواده LTO آندهای از جنس TiO2 هم مطرح است. سنتز این آندها راحتتر است، بهعلاوه چون مرحله واکنش با پیش ماده لیتیومدار در اثر حرارت را نمیخواهند، مشکلات ناشی از حرارت مثل رشد نانومواد را ندارند. بهعلاوه بر اساس فرمول شیمیایی، اکسید تیتانیوم دارای ظرفیت دو برابر مقدار 335mAh/g) LTO) است. واکنش کلی این آندها به صورت است.
TiO2 دارای 4 نوع فاز یا ساختار کریستالوگرافی (چینش اتمی متفاوت) معروف با نامهای بروکایت، آناتاز، روتایل و (TiO2(B است. فاز بروکایت برای باتری اهمیتی ندارد. آناتار و روتایل که فازهای خیلی معروف هستند، بهعنوان آند دارای اهمیت هستند. فاز (TiO2(B بدلیل فضای باز اتمی و کانال مناسب برای انتقال یون، عملکرد بهتری از دیگران دارد و بیشتر از همه مورد توجه است.
اگر ظرفیت تئوری را بر مبنای فرمول شیمیایی (به ازای هر مول TiO2، یک مول یون لیتیوم) در نظر بگیریم، برابر مقدار فوقالذکر است ولی بر مبنای فاز و جایگاهی که با توجه به شبکه کریستالی یون لیتیوم میتواند قرار گیرد، ظرفیتهای تئوری متفاوتی برای فازهای مختلف گزارش شده است؛ مثلا برای آناتاز با توجه به جایگاههای شبکه، ظرفیت نصف مقدار بالا یعنی 0.5 مول یون لیتیوم به ازای هر مول TiO2 یعنی 167mAh/g است (مرجع همان نانوصفحهها).
چون تمام این فازها رسانایی یونی ضعیف دارند، ابعاد نانو هم در افزایش توان و هم ظرفیت بسیار موثر است که در مقالات فراوانی مورد بحث قرار گرفته است. اما آنچه جالب توجه است ظرفیت نانوساختار آناتاز از ظرفیت تئوری بر مبنای جایگاه شبکه بیشتر است ولی حتما در همه فازها از ظرفیت تئوری فرمولی 334 کمتر است.
روتایل در حالت میکرونی فقط توانایی ذخیره 0.1 مول یون لیتیوم را به ازای واحد شبکه دارد. در روتایل مکانهای قرارگیری لیتیوم در کل شبکه قرار دارد ولی ضریب نفوذ در جهت محور c نسبت به صفحه ab یک مرتبه بزرگتر است. اتم لیتیوم در جهت محور c خوب نفوذ میکند ولی باید از طریق نفوذ در صفحه ab در کل فضا پخش شود و چون در صفحه ab سرعت نفوذ پایین است، بنابراین تجمع یونهای لیتیوم در کانال c صورت میگیرد که موجب میشود یک نیروی دافعه ناشی از بار مثبت یون لیتیوم ایجاد شود. این نیروی دافعه از ورود بیتشر یونها به داخل شبکه جلوگیری میکند. بهعنوان یک نتیجه جالب از اثر نانو مشخص شده که وقتی ابعاد روتایل نانو میشود ظرفیت تا مقدار 0.8 مول یون لیتیوم میرسد که این ظرفیت در طول سیکلهای مختلف برگشتپذیری هم دارد که علت کاهش مسافت نفوذ و اثر توان دوم آن است (مراجعه شود به مقاله 4) و در این حالت تجمع و نیروی دافعه وجود ندارد. شکل 4 منحنی شارژ و دشارژ و طول عمر سیکلی را برای روتایل بالک (میکرونی)، نانوذرات تجاری میکرونی روتایل و نانوسیمهای روتایل نشان میدهد. همانطور که دیده میشود نانوسیمها طول عمر سیکلی و ظرفیت خوبی را نشان میدهند. شکل تایید کننده این مطلب هم هست که شکل نانومواد نیز در عملکرد آند موثر است.
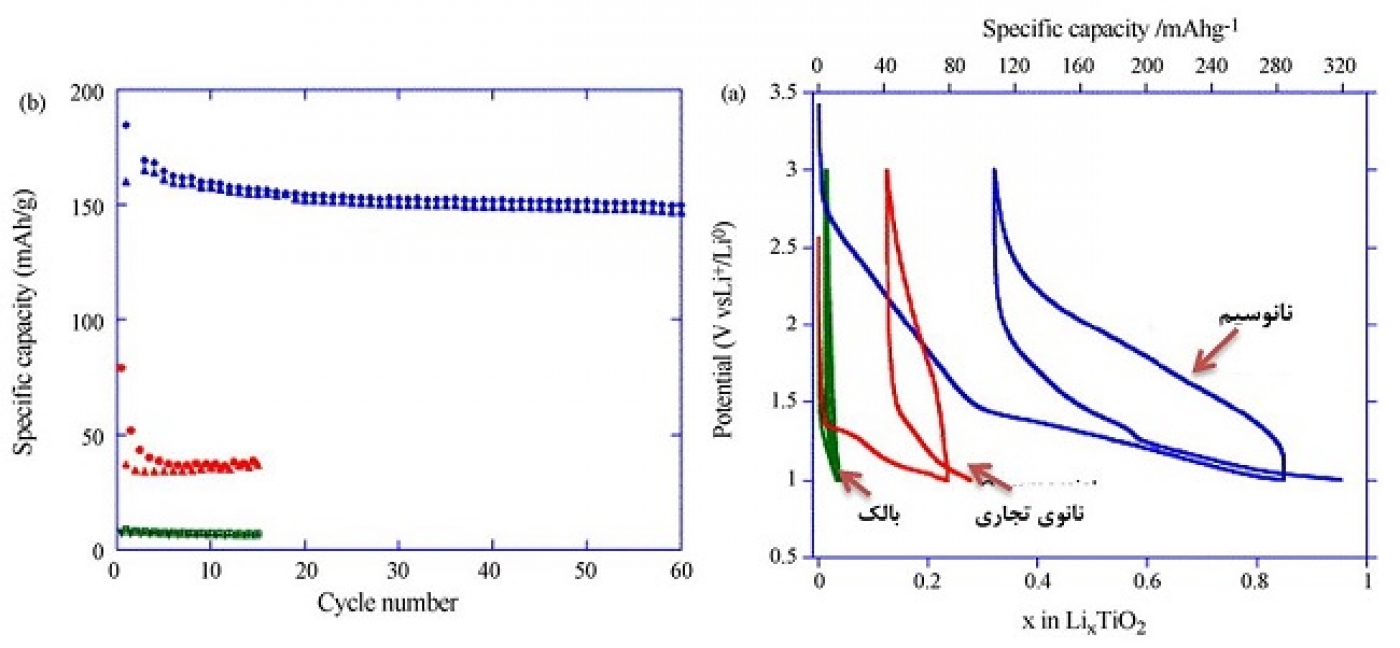
شکل 4-a- منحنی شارژ-دشارژ اولین بار، b- طول عمر سیکلی
موروفولوژی مثلا نانوذره، نانوسیم و ... هم در ظرفیت، و هم در طول عمر سیکلی و توان تفاوت دارند ولی نوع مورفولوژی به تنهایی تعیینکننده نیست بلکه هندسه ساختار است که عملکرد را مشخص میکند (در آینده درباره هندسه ساختار برای همه مواد فعال صحیت میشود)، مثلا نانوسیم متصل به جمعکننده جریان، نانوسیم مخلوط با گرافن و نانوسیم ایزوله هر کدام نتیجه متفاوتی را ارایه میدهند. بهعلاوه شرایط تست و نرخ C و عوامل فراوان دیگری هم وجود دارند که با توجه به همه اینها، بهراحتی نمیتوان نتایج مقالات را با یکدیگر مقایسه کرد.
فاز (TiO2(B که نسبت به فازهای دیگر، جدیدتر مورد توجه قرار گرفته است، بدلیل داشتن کانالهای مناسب برای انتقال یون لیتیوم، بهترین توان و ظرفیت را ارایه میدهد. شکل ساختار مکان نفوذ را نشان میدهد. وقتی ابعاد در جهت نفوذ نانو میشود ظرفیت به مقدار قابل توجهی بیشتر میشود. این فاز در بین تمام آندهای تیتانیومی از جمله LTO، بهترین توان و ظرفیت را ارایه میدهد به طوری که با نانو کردن آن تنها در 4.5 ثانیه، آند با ظرفیت 73 درصد تئوری شارژ یا دشارژ میشود، در این آند نیز تغییر حجم نداریم.
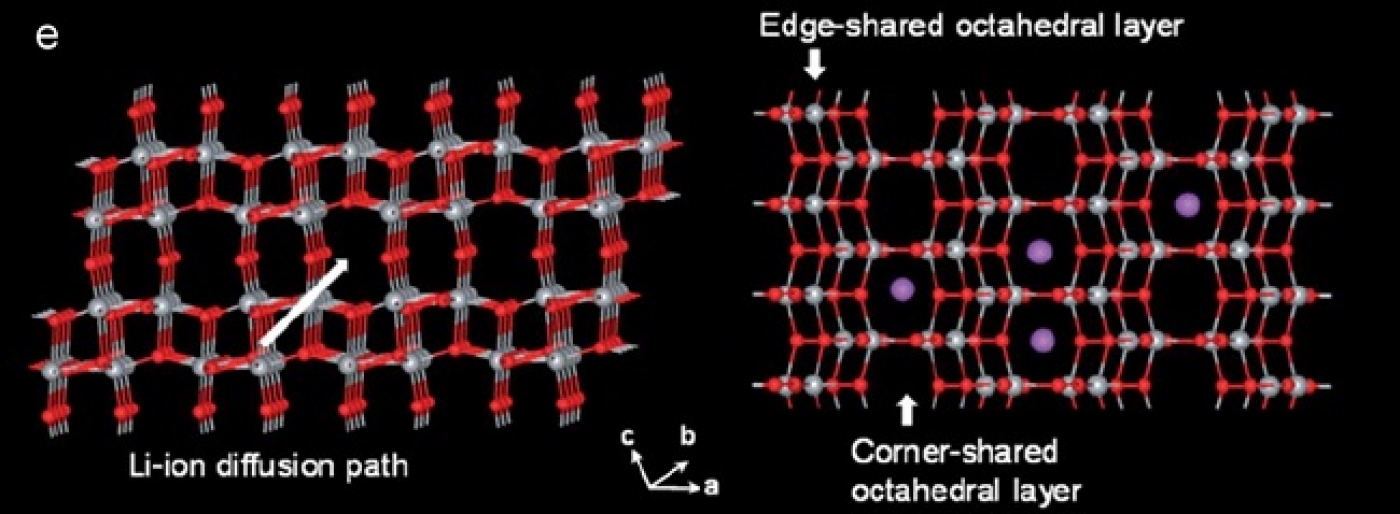
شکل 5- نمایش ساختار اتمی فاز (TiO2(B
3- ظرفیت شبه خازنی
تا کنون درباره ظرفیت ناشی از ذخیره یون لیتیوم به شکل درجی درون شبکه اتمی بحث و مشاهده شد که این ظرفیت در ابعاد نانو بدلیل کاهش مسافت نفوذ و ... بهبود مییابد. اما یکی از پدیدههای جالبی که برای این آندها در ابعاد نانو رخ میدهد ذخیره یون لیتیوم در سطح ناشی از نسبت سطح به حجم فراوان است. این نوع ذخیرهسازی متفاوت از ظرفیت درجی و آلیاژی است که تا بهحال گفته شد. این نوع ذخیرهسازی بهدلیل اینکه نیاز به نفوذ ندارد خیلی سریع است و همچنین چون تنش و مانند آن ایجاد نمیکند بهترین طول عمر سیکلی و توان را در مقایسه با دیگر روشهای ذخیره لیتیوم دارد. البته این نوع ظرفیت مقدار انرژی کمتری را ایجاد میکند. درباره این ظرفیت به طور کاملتر در مبحث ابرخازنها صحبت میشود. شکل، مقایسهای بین مقدار ذخیرهسازی ظرفیت LTO را در سه بعد مختلف نانو نشان میدهد. با توجه به شکل در ابعاد کوچک نانو این ظرفیت قابل توجه است و با افزایش ابعاد کاهش قابل ملاحظهای مییابد. باید این نکته را ذکر کرد که ظرفیت خازنی فقط مربوط به ترکیبات اکسید تیتانیوم نمیشود بلکه در خیلی مواد فعال دیگر موجود است که در هنگام معرفی آنها گفته میشود.
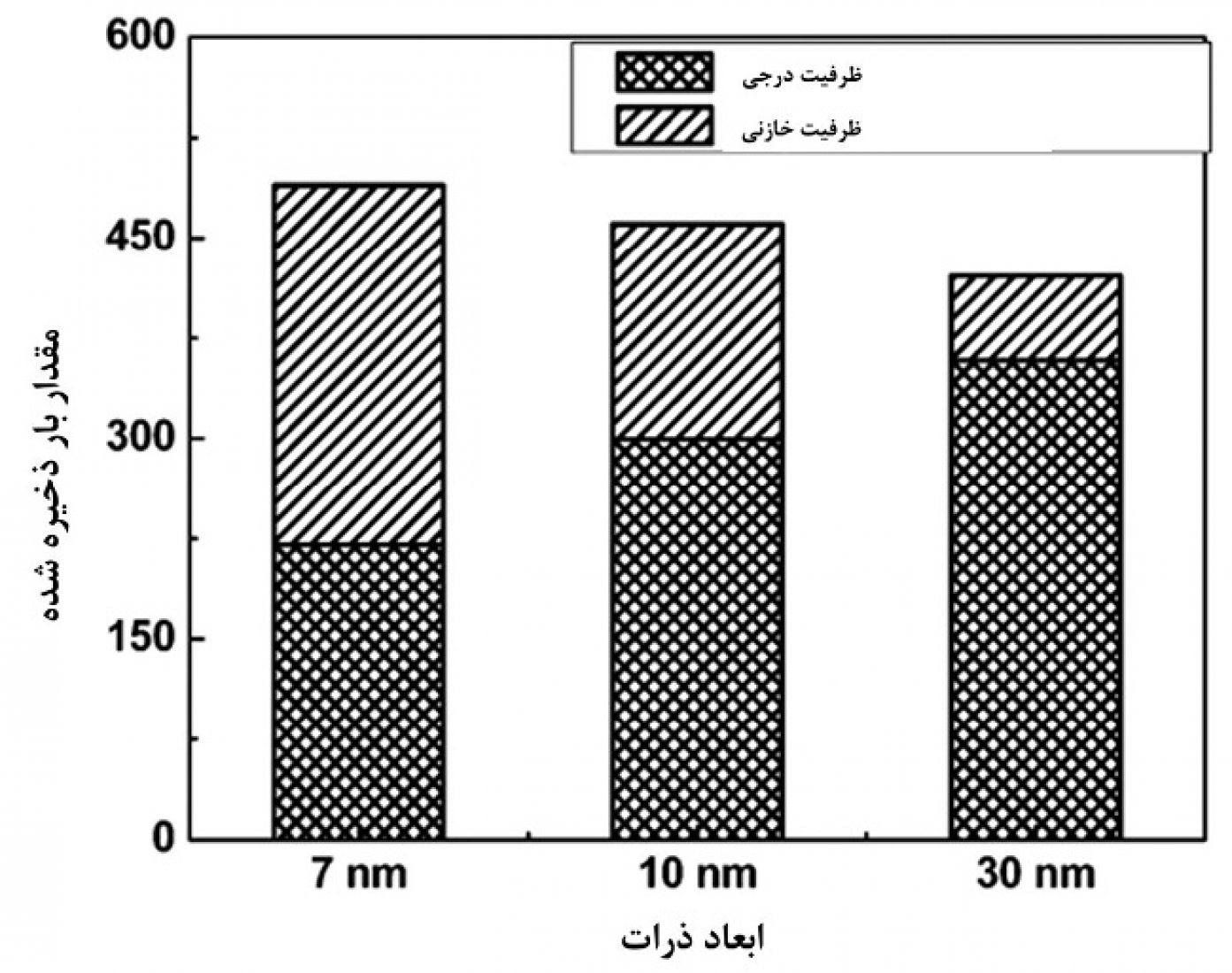
شکل 6- نمایش ظرفیتهای درجی و ابرخازنی در اکسید تیتانیوم
4- جمعبندی و نتیجهگیری
پوشش کربنی بر روی آند میتواند رسانایی را از مقدارS/cm10-13 به مقدار 2.05S/cm برساند. درباره پوششهای کربنی و دیگر افزودنیهای رسانا در مقالات آتی برای مواد فعال بحث میشود. دوپینگ با افزایش رسانایی الکترونی و حتی یونی و فراهم کردن فضای بیشتر درون شبکه به همراه نانوسایز کردن میتواند عملکرد را ارتقا دهد (مثال مرجع 9) که برای پروژههای جدید شاید مناسب باشد که بیشتر یک مبحث نانویی در زمینه سنتز نانوست تا چگونه ماده را همراه با دوپینگ در ابعاد نانو سنتز کنیم تا اینکه یک بحث درباره اثر نانو در بهبود عملکرد آند باشد.
در این مقاله درباره آندهای اکسید تیتانیوم که یکی از مهمترین آندها از جنبه تجاری است صحبت شد. مشخص شد که نانوفناوری بهبود فراوانی در عملکرد این آندها ایجاد میکند. همچنین معلوم شد نانوسایز کردن حتی ماهیت الکتروشیمیایی و شیمی-فیزیکی را (همانند تغییر شکل منحنی شارژ-دشارژ و ظرفیت بیشتر در لایههای سطحی) تحت تاثیر قرار میدهد. توصیه میشود تا سوالات آزمون این مقاله حتما مورد مطالعه قرار گیرد تا مطالب بهتر درک شود. در آخر با توجه به پیچیده بودن مطالب خواهشمند است در صورت وجود ابهام سوالات خود را حتما بیان کنید.
منابـــع و مراجــــع
۱ - Wu, Hui, et al. "Stable cycling of double-walled silicon nanotube battery anodes through solid-electrolyte interphase control." Nature nanotechnology 7.5 (2012): 310-315.
۲ - . Liu, Nian, et al. "A yolk-shell design for stabilizedscalable Li-ion battery alloy anodes." Nano letters 12.6 (2012): 3315-3321.
۳ - Pinson, Matthew B.,Martin Z. Bazant. "Theory of SEI formation in rechargeable batteries: capacity fade, accelerated aginglifetime prediction." Journal of The Electrochemical Society 160.2 (2013): A243-A250.
۴ - Nie, Mengyun. Anode solid electrolyte interphase (SEI) of lithium ion battery characterized by microscopyspectroscopy. Diss. University of Rhode Island, 2014.
۵ - Ganapathy, Swapna,Marnix Wagemaker. "Nanosize storage properties in spinel Li4Ti5O12 explained by anisotropic surface lithium insertion." ACS nano 6.10 (2012): 8702 8712.
۶ - Okumura, Toyoki, et al. "Nanosized Effect on Electronic/Local StructuresSpecific Lithium-Ion Insertion Property in TiO2–B Nanowires Analyzed by X-ray Absorption Spectroscopy." Chemistry of Materials 23.16 (2011): 3636-3644.
۷ - Borghols, W. J. H., et al. "Size Effects in the Li4+ x Ti5O12 Spinel." Journal of the American Chemical Society 131.49 (2009): 17786-17792.
۸ - Wang, John, et al. "Pseudocapacitive contributions to electrochemical energy storage in TiO2 (anatase) nanoparticles." The Journal of Physical Chemistry C 111.40 (2007): 14925-14931.
۹ - Ma, Yue, et al. "Carbon-encapsulated F-doped Li4Ti5O12 as a high rate anode material for Li+ batteries." ACS nano 7.12 (2013): 10870-10878.
۱۰ - Wang, Feng, et al. "Excess lithium storagecharge compensation in nanoscale Li4+ xTi5O12." Nanotechnology 24.42 (2013): 424006.

